管理臨床試驗文件 數碼簽署






臨床試驗文件管理的挑戰
在製藥和生物技術行業,臨床試驗是創新的基石,但它們也帶來了巨大的行政負擔。管理臨床試驗文件——從知情同意書和病例報告表(CRFs)到方案修正案和不良事件報告——需要精確性、安全性和合規性,以滿足嚴格的監管標準。文件處理中的延誤可能導致昂貴的挫折、倫理問題,甚至試驗中止。從商業角度來看,低效的文件管理會增加營運成本,據德勤和麥肯錫的行業報告顯示,糟糕的流程會導致高達30%的試驗延誤。
關鍵挑戰包括版本控制,其中單個文件的多個迭代必須被追蹤以避免錯誤;全球站點間的安全共享,因為試驗往往跨越大陸;以及審計就緒的可追溯性,以滿足監管要求。例如,確保同意書上的每個簽名都是可驗證的並帶有時間戳是不可談判的。沒有強大的系統,團隊依賴手動工作流程,如打印、掃描和快遞,這不僅會減緩進度,還會增加數據洩露或不合規的風險。在高風險環境中,一個小小的疏忽可能危及患者安全或知識產權,企業越來越多地轉向數字工具來簡化這些流程。
電子簽名已成為變革性的工具,能夠實現遠程簽名,同時保持法律可執行性。然而,選擇正確的平台需要平衡諸如審計追蹤、與電子數據捕獲(EDC)系統的集成以及遵守全球法規等功能。這種轉變不僅加速了試驗時間線——可能縮短20-25%——還降低了與紙質物流相關的成本。

電子簽名在臨床試驗中的作用
電子簽名(e-signatures)透過提供數字審計追蹤來解決臨床試驗文件管理的核心痛點,該追蹤記錄了誰簽名、何時簽名以及如何簽名。在FDA的21 CFR Part 11等框架下,電子簽名必須確保記錄值得信賴、可靠,並等同於濕墨簽名。該法規對美國試驗至關重要,要求防止偽造的控制措施,包括電子時間戳和用戶認證。在歐洲,eIDAS法規為合格電子簽名(QES)設定了類似標準,強調跨境有效性。
對於跨國試驗,區域差異增加了複雜性。在亞太(APAC)市場,試驗正在快速增長——據IQVIA預測,到2025年將佔全球活動的25%——當地法律要求量身定制的合規性。新加坡的《電子交易法》承認電子簽名具有證據效力,而香港的《電子交易條例》與國際規範一致,但需要與國家ID系統集成以獲得更高保障。日本的《個人信息保護法》進一步強調數據本地化。企業必須選擇支持這些法規的平台,而不損害速度或可擴展性。
從商業角度來看,電子簽名在臨床試驗中的採用帶來了可衡量的投資回報:透過遠程同意加快患者招募、降低現場訪問成本,以及透過基於雲的儲存庫提升協作。然而,與Veeva或Medidata等試驗管理軟件的集成至關重要,以避免孤島。
臨床試驗的關鍵電子簽名提供商
DocuSign
DocuSign 是電子簽名解決方案的市場領導者,在臨床研究中廣泛採用,因其強大的合規功能。它支持21 CFR Part 11,提供詳細的審計日誌、生物識別認證和信封級安全,使其適合敏感的試驗文件。企業欣賞其與EDC平台和CRM系統的無縫集成,促進從方案批准到現場啟動的工作流程。定價從基本計劃的每月每用戶約10美元開始,對於企業功能如批量發送和API訪問會相應增加。雖然其全球覆蓋範圍強大,但一些APAC用戶指出,由於美國中心的基礎設施,偶爾會出現延遲。

Adobe Sign
Adobe Sign 作為Adobe Document Cloud的一部分,在文件中心工作流程中表現出色,提供AI驅動的編輯和表單填充功能,簡化CRF管理。它符合21 CFR Part 11和eIDAS,具有多因素認證和加密儲存等功能,吸引製藥合規官。與Adobe Acrobat的集成提升了編輯能力,適合註釋試驗方案。定價分級,從每月每用戶10美元開始,但高級合規附加組件可能會增加成本。它對已在Adobe生態系統中的團隊特別友好,儘管針對APAC特定ID的自定義可能需要額外配置。

HelloSign (by Dropbox)
HelloSign 現在集成到Dropbox中,提供了一個注重簡單性和安全性的直觀電子簽名工具。它透過防篡改封印和基於角色的權限滿足21 CFR Part 11要求,適合同意書和研究者協議。其API允許嵌入到試驗應用中,免費層級使其適用於較小的研究。定價從每月每用戶15美元開始,更高計劃提供無限模板。雖然適用於基本需求,但它可能缺乏企業級功能如高級分析,將其定位為中型生物技術公司的經濟實惠選擇。
eSignGlobal
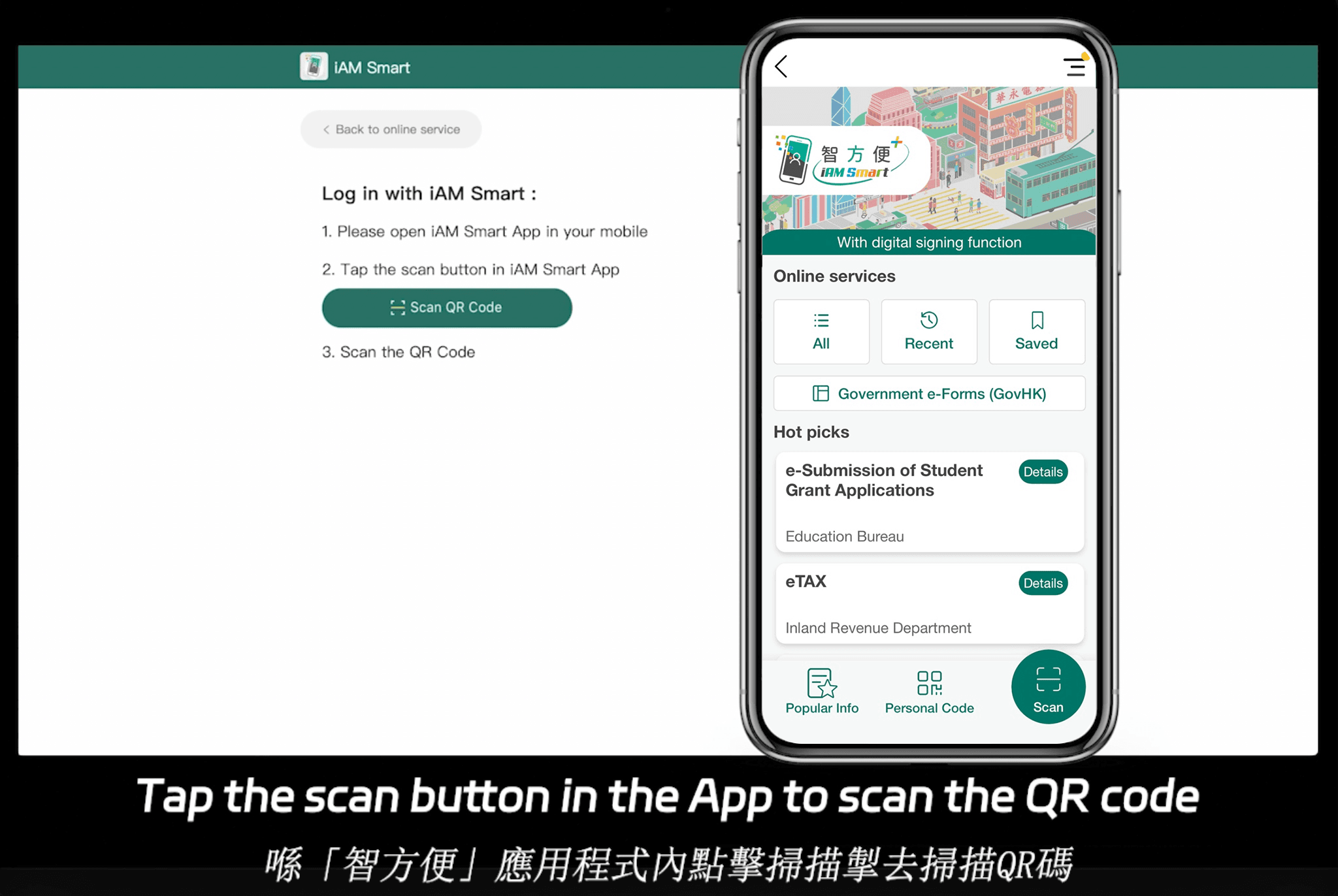
eSignGlobal 以專注於APAC合規性而脫穎而出,支持全球超過100個主流國家的電子簽名,同時在區域適應方面表現出色。它遵守21 CFR Part 11、eIDAS、ESIGN/UETA以及當地APAC法律,提供諸如與香港iAM Smart和新加坡Singpass的無縫集成以驗證身份等優勢。這對於這些樞紐的試驗特別有價值,確保法律可執行性而無管轄障礙。在定價方面,其模式強調實惠性——詳情請查看eSignGlobal的定價頁面——Essential計劃僅為每月16.6美元,允許最多100份簽名文件、無限用戶席位,並透過訪問碼驗證。這種無席位費結構在合規基礎上提供高成本效益,使其對價格敏感市場的擴展團隊具有吸引力。
電子簽名平台的比較分析
為了輔助決策,以下是基於臨床試驗需求的關鍵提供商的中立比較:
| 功能/方面 | DocuSign | Adobe Sign | eSignGlobal | HelloSign (Dropbox) |
|---|---|---|---|---|
| 合規性 (21 CFR Part 11, eIDAS) | 全面支持,帶有審計追蹤 | 強大,AI增強安全 | 全球(100+國家),APAC重點 | 基本支持,防篡改 |
| APAC集成 (例如 Singpass, iAM Smart) | 有限,需要附加組件 | 部分,可配置 | 原生且無縫 | 最小 |
| 定價 (入门級,美元/月) | $10/用戶 | $10/用戶 | $16.6 (無限用戶) | $15/用戶 |
| 文件限制 (基本計劃) | 每月5-10個信封 | 無限,但有儲存費 | 100份文件 | 無限模板,按使用付費 |
| 試驗關鍵優勢 | 企業集成 | 文件編輯工具 | 成本效益無限用戶 | 簡單性和Dropbox協同 |
| 局限性 | 擴展時成本更高 | 生態系統鎖定 | 在某些西方市場較新 | 高級分析較少 |
此表格突出了權衡:像DocuSign這樣的全球巨頭提供廣度,而像eSignGlobal這樣的區域玩家優先考慮本地化效率。
實施最佳實踐
在臨床試驗中實施電子簽名從合規審計開始,將文件映射到法規。培訓團隊使用工作流程,例如使用模板處理重複表單,以將準備時間縮短50%。監控簽名完成率等指標以優化流程。對於跨國設置,混合模型——結合雲和本地部署——平衡可訪問性和數據主權。企業應使用樣本試驗數據試點平台以評估適用性。
在APAC,試驗強調速度以應對競爭格局,具有低延遲本地數據中心的平台可降低監管審查風險。最終,選擇取決於試驗規模、預算和地理位置——確保工具提升而非複雜化管理。
作為DocuSign的區域合規需求中立替代方案,eSignGlobal為APAC重點試驗提供了一個引人注目的選擇。
常見問題




