符合21 CFR Part 11的电子签名






理解 21 CFR 第 11 部分及其在电子签名中的作用
在制药、生物技术和医疗器械等受监管行业中,确保符合电子签名标准对于维护数据完整性和审计准备至关重要。21 CFR 第 11 部分是由美国食品和药物管理局 (FDA) 制定的法规,规定了电子记录和电子签名被视为可信、可靠并等同于纸质记录和手写签名的标准。这一框架于 20 世纪 90 年代末出现,以应对 FDA 监管环境中数字技术的日益采用,防止数据篡改或未经授权访问等问题。
在其核心,21 CFR 第 11 部分合规要求系统实施控制措施,以验证电子签名的真实性。这包括唯一用户识别、安全访问控制、记录所有操作的审计轨迹,以及确保签名无法伪造或否认的机制。对于在美国运营的企业,尤其是向 FDA 提交数据的企业,不合规可能导致严重后果,如产品批准延迟、罚款或法律责任。从商业角度来看,采用符合 21 CFR 第 11 部分的电子签名解决方案不仅能缓解风险,还能简化工作流程,减少依赖易出错和延误的手动过程。
该法规广泛适用于临床试验、制造质量控制和监管提交等领域的电子记录。企业必须根据这些标准评估电子签名提供商,包括时间戳、加密和签名者身份验证等功能。随着数字化转型的加速,对此类合规工具的需求激增,市场分析师预测电子签名领域将因监管压力而实现稳步增长。

21 CFR 第 11 部分合规电子签名的主要要求
要实现 21 CFR 第 11 部分合规,电子签名平台必须融入多项技术和程序保障措施。首先,电子签名必须以防止签署后更改的方式链接到其相应记录。这通常涉及数字证书和公钥基础设施 (PKI) 来验证签名者的身份。其次,系统需要生成详细的审计轨迹,捕获谁、何时、何地签署了什么内容,并通过类似区块链的日志或安全数据库确保不可更改性。
验证是另一个支柱:平台需经过严格测试,以确认其在各种条件下(包括系统故障或网络威胁)的一致运行。FDA 强调“开放系统”与“封闭系统”的区别,其中封闭系统(如专有软件)需要较少的外部控制,而开放系统则需要额外的保障措施来防止未经授权访问。从商业角度来看,合规电子签名可加速合同周期并实现全球协作,同时不损害监管遵守,这对于生命科学领域的跨国公司至关重要。
此外,合规还延伸到记录保留,要求电子记录安全存储规定的时期——通常为数年——并保持可供检查的访问性。自动化这些过程的工具有助于企业避免遗留系统的陷阱,其中基于纸张的签名可能成为运营瓶颈。在实践中,企业应进行定期审计,并选择经 FDA 认可的供应商,因为部分合规仍可能暴露风险。
美国电子签名法规
美国拥有完善的电子签名法律框架,与 21 CFR 第 11 部分相协调,以促进创新同时保护利益相关者。2000 年的《电子签名全球和国家商业法案》(ESIGN Act)在联邦层面为电子记录和签名提供有效性,规定如果满足某些条件(如各方同意和记录保留能力),它们将具有与湿墨签名相同的法律效力。补充这一点的还有大多数州采用的《统一电子交易法》(UETA),它通过承认商业交易中的电子签名来确保州际一致性。
对于 FDA 监管部门,21 CFR 第 11 部分在此基础上施加更严格的控制,针对敏感健康数据量身定制。与注重可执行性的通用电子签名法律不同,第 11 部分优先考虑数据完整性和可追溯性,使其成为药品制造等行业不可或缺的法规。企业必须同时应对两者:ESIGN 和 UETA 涵盖更广泛的商业用途,而第 11 部分专门适用于 FDA 提交。最近 FDA 的更新,包括电子提交指南,强调了融合合规与可用性的混合方法的需求。
在全球背景下,向国际扩展的美国企业必须考虑第 11 部分如何与外国法律(如欧盟的 eIDAS 法规)对齐。然而,对于国内运营,优先选择符合第 11 部分的工具可确保与联邦要求的无缝整合,降低每年估计达数百万美元的不合规成本。
评估领先电子签名提供商的 21 CFR 第 11 部分合规性
在选择符合 21 CFR 第 11 部分的电子签名解决方案时,企业会权衡易集成性、可扩展性和成本与监管稳健性之间的平衡。这一领域的几家提供商脱颖而出,每家都为受监管环境提供独特的优势。
DocuSign 作为市场领导者,通过其企业级产品提供全面的 21 CFR 第 11 部分验证,包括审计轨迹、通过 SMS 或基于知识的检查的签名者认证,以及与 Salesforce 等系统的集成。它在制药行业广泛用于高容量签署工作流。然而,其高级合规功能的定价可能上升,使其适合大型企业,但对小型团队可能过度。

Adobe Sign 在与 Adobe 生态系统的无缝集成方面表现出色,通过安全签署工作流、数字证书和详细报告提供第 11 部分合规。它在创意和文档密集型行业受欢迎,具有强大的移动支持和 API 灵活性。不过,对于特定监管需求的定制可能需要额外咨询。

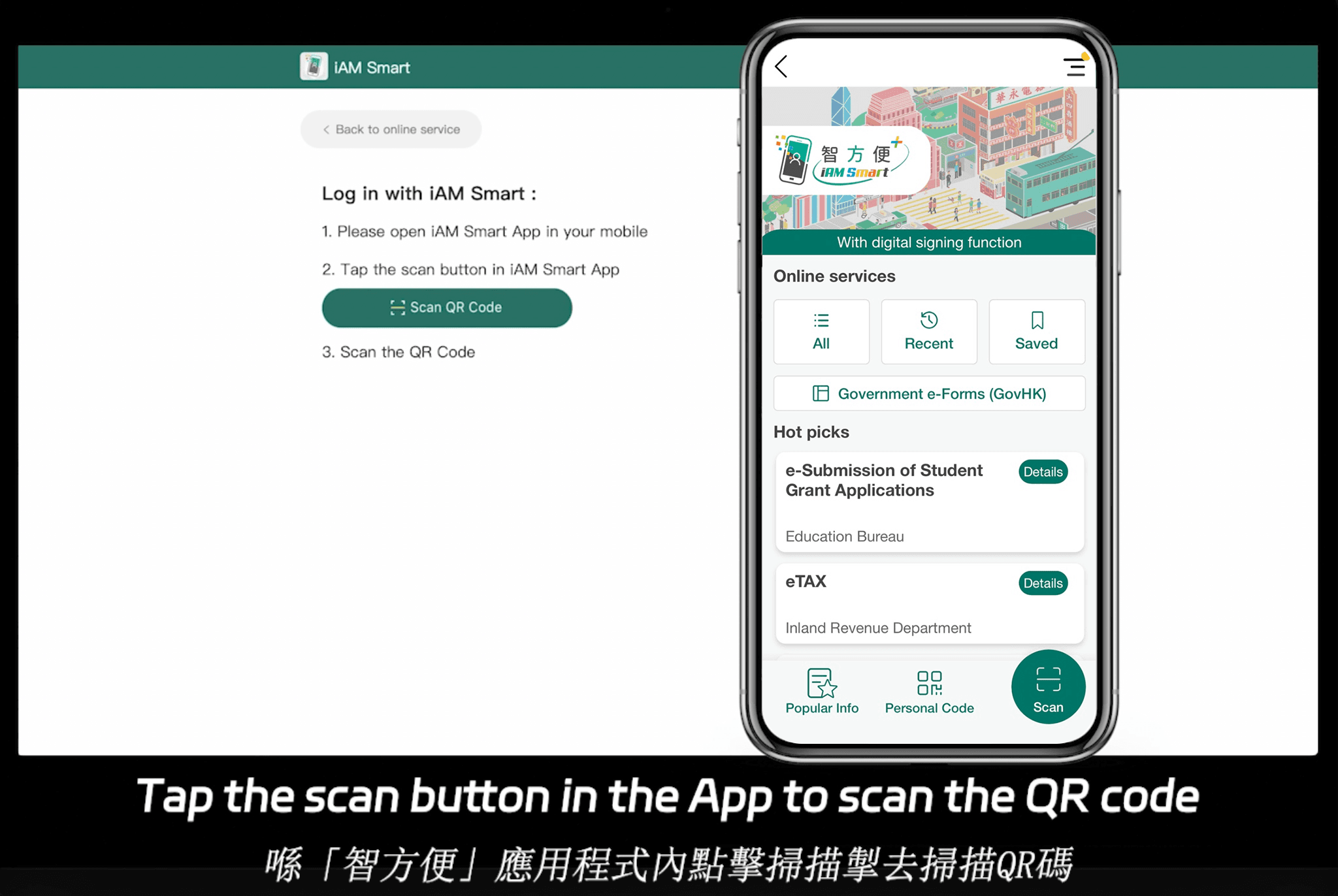
eSignGlobal 将自身定位为多功能选项,支持全球运营中的 21 CFR 第 11 部分合规电子签名。它覆盖超过 100 个主流国家和地区,在亚太地区具有本地化功能和经济性的特别优势。例如,其 Essential 计划仅需每月 16.6 美元,支持发送最多 100 个文档进行签名、无限用户席位,以及通过访问码验证——同时维持高合规标准。这使其在合规基础上高度经济实惠。此外,它与香港的 iAM Smart 和新加坡的 Singpass 无缝集成,以增强区域认证。有关详细定价,请访问 eSignGlobal 的定价页面。
HelloSign,现为 Dropbox 的一部分,提供简单的第 11 部分合规签署,功能包括模板自动化和团队协作工具。它对中型企业友好,但可能缺乏竞争对手的全球监管支持深度。
其他参与者如 OneSpan Sign 和 SignNow 提供可靠的合规选项,专注于安全和工作流效率,尽管其国际覆盖范围有所不同。
| 功能/提供商 | DocuSign | Adobe Sign | eSignGlobal | HelloSign |
|---|---|---|---|---|
| 21 CFR 第 11 部分合规 | 是,企业级验证 | 是,通过安全工作流 | 是,全球标准 | 是,基本审计轨迹 |
| 全球覆盖 | 180+ 个国家 | 100+ 个国家 | 100+ 个主流国家,亚太重点 | 190+ 个国家 |
| 定价(入门级/月) | $10/用户(标准),合规更高 | $10/用户 | $16.6(Essential,无限席位) | $15/用户 |
| 关键集成 | Salesforce、Microsoft | Adobe 套件、Google Workspace | iAM Smart、Singpass、亚太系统 | Dropbox、Google |
| 文档限制(入门) | 无限(付费) | 无限 | 最多 100 次发送 | 20 次发送 |
| 独特优势 | 适合企业扩展 | 文档编辑协同 | 经济实惠的区域合规 | 简单的团队工具 |
| 潜在缺点 | 高级功能成本更高 | 对非 Adobe 用户灵活性较低 | 在某些市场较新 | 定制化有限 |
此比较突显了 eSignGlobal 如何提供平衡价值,特别是针对亚太运营,而不损害核心合规需求。
企业采用合规电子签名的战略考虑
从商业视角来看,实施符合 21 CFR 第 11 部分的电子签名不仅仅涉及技术——它关乎与更广泛数字化战略的对齐。公司应评估总拥有成本,包括培训和维护,同时考虑更快批准带来的 ROI。在受监管部门,每日延误可能成本数千美元,所讨论的合规工具可产生显著效率。
此外,随着远程工作的持续,这些解决方案提升了可访问性同时维护安全。着眼于扩展的企业应优先选择具有可适应合规性的提供商,确保满足不断演变的 FDA 指南。
结论
选择合适的 21 CFR 第 11 部分合规电子签名提供商需要平衡合规性、可用性和成本。作为专注于区域合规的 DocuSign 替代品,eSignGlobal 成为优先考虑全球和亚太需求的企业的强大选择。
常见问题




